科辰星飞小动物活体成像系统助力ALI/ARDS治疗新篇章
摘要:急性肺损伤(ALI)及其恶化形式急性呼吸窘迫综合征(ARDS)是临床上的重大挑战,全球每年影响数百万患者,且目前缺乏有效的治疗手段。近期,一项研究通过开发一种创新的双管齐下纳米平台,成功在ALI小鼠模型中恢复了肺泡上皮细胞(AECs)的功能,阻断了肺纤维化的进程。这一突破性的研究成果不仅为ALI/ARDS的治疗提供了新的思路,还巧妙地运用了科辰星飞多功能荧光成像系统(LumiFluor AVIS T II)进行成像,为实验的精准分析与验证提供了强有力的技术支持。


导言中的新视角
急性肺损伤(ALI)及急性呼吸窘迫综合征(ARDS)作为重症监护室(ICU)中的常见且致死率高的综合征,其治疗手段的匮乏一直是医学界亟待解决的问题。肺泡上皮细胞(AECs)的损伤与死亡是ALI/ARDS病理过程中的关键环节,而如何有效干预这一过程,减少AECs的损伤,促进其功能恢复,成为了研究的热点。
研究背景与挑战
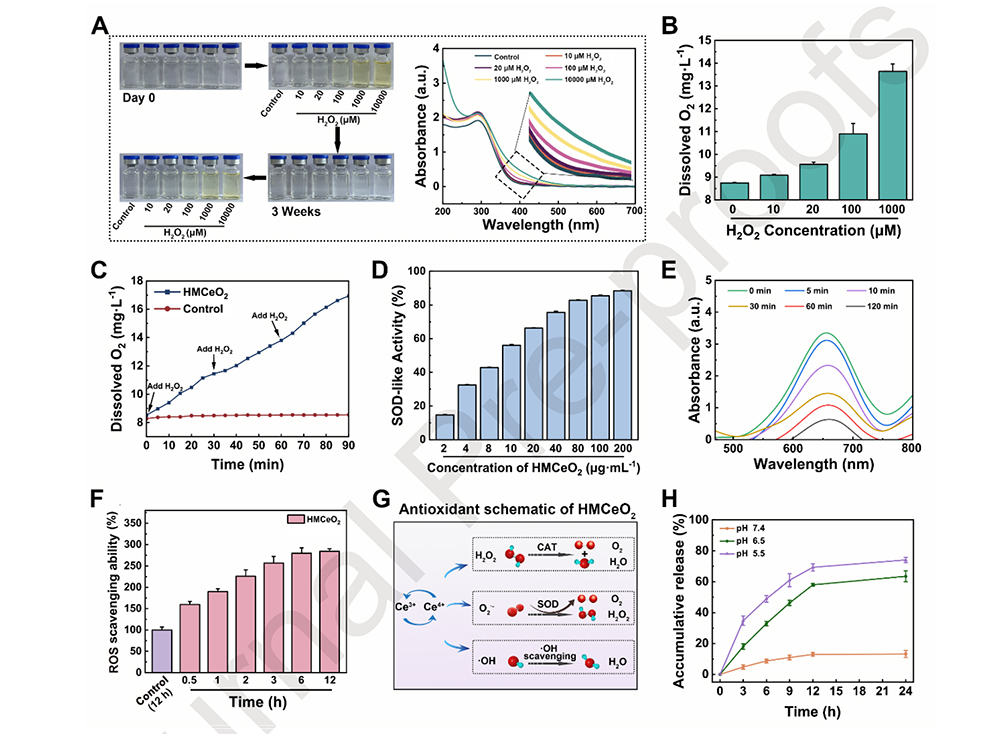
肺泡上皮细胞,包括1型肺泡上皮细胞(AEC1s)和2型肺泡上皮细胞(AEC2s),是维持肺泡-毛细血管屏障功能的核心。细菌病原体入侵后,AECs遭受ROS、钙超载及炎症信号的多重打击,导致细胞凋亡和炎症途径的激活,最终破坏肺泡-毛细血管屏障,甚至引发肺纤维化。因此,开发一种能够同时清除ROS、消除钙超载、抑制炎症的治疗策略显得尤为重要。

科辰星飞多功能荧光成像系统助力创新研究
在这项研究中,科研团队创新性地设计了一种双管齐下的纳米平台,该平台结合了中空介孔CeO2纳米颗粒(HMCeO2 NPs)与MDA-MB-231细胞膜(M231 M)的仿生特性,以及RAGE拮抗剂多肽(RAP)的抗炎作用。这一复合纳米制剂不仅能够有效靶向肺泡基底膜,还能从细胞内和细胞外两个层面同时发挥抗凋亡和抗炎作用。

细胞内作用机制:HMCeO2 NPs与膜渗透性钙螯合剂BAPTA-AM(BA)的结合,通过M231 M包裹形成仿生HMCeO2-BA@M231 M NPs。这一设计使得纳米粒子能够进入AECs,消耗ROS并释放O2.同时螯合细胞内过量的钙离子,恢复线粒体裂变-融合平衡,抑制细胞凋亡。
细胞外作用机制:在M231 M表面装饰RAP,形成RAP-M231 M NPs,其表面的RAP能够与损伤AECs膜上高表达的RAGE结合,阻断炎症信号通路的激活,减少促炎细胞因子的产生。
为了验证这一复合纳米平台的疗效及其作用机制,研究团队采用了科辰星飞多功能荧光成像系统(LumiFluor AVIS T II)进行成像。该系统以其高分辨率、高灵敏度和多通道成像能力,为研究人员提供了清晰的细胞内外动态变化图像,使得纳米粒子在肺泡基底膜的靶向富集、AECs内的分布以及线粒体形态的变化等关键信息得以直观展现。

实验成果与临床应用前景
通过LumiFluor AVIS T II的精准成像,研究团队观察到,单剂量施用复合纳米平台后,ALI小鼠的肺部结构和功能得到了显著恢复,存活率从73.3%提高到了100%。更重要的是,这一治疗策略加速了AEC2向AEC1的转化,从根本上阻止了ALI晚期的肺纤维化进程。
这一研究成果不仅为ALI/ARDS的治疗提供了新的思路,也为科辰星飞多功能荧光成像系统在生物医学研究中的应用展示了广阔的前景。LumiFluor AVIS T II的高性能成像能力,为纳米药物在细胞内的动态分布、作用机制及疗效评估提供了强有力的技术支持,加速了基础研究成果向临床应用的转化。
总结
综上所述,科辰星飞多功能荧光成像系统(LumiFluor AVIS T II)在这一创新研究中的应用,不仅验证了双管齐下纳米平台在治疗ALI/ARDS中的巨大潜力,也展示了其在生物医学成像领域的独特优势。随着研究的深入和技术的不断进步,相信这一复合纳米平台将有望成为ALI/ARDS治疗的新选择,为更多患者带来希望。科辰星飞也将继续致力于提供高质量的科研工具,助力生物医学研究的不断发展与创新。
